|
第六章
多原子分子(二)
Chapter 6. The polyatomic molecules(B)
§6.1 缺电子多中心键(Electron-deficient multi-center bonds)
上几节介绍的离域π键,是价电子较多的原子形成的分子,除了形成σ键,还有多余的电子可形成离域π键。而这一节要讨论的是一些价电子缺乏,多个原子共用电子对的多中心键,在硼烷、金属烷基化合物中常存在这种缺电子多中心键。
一.硼烷
硼烷的结构
早期对硼烷B2H6的结构有很长时间的争论,一种意见认为B2H6类似乙烷的结构,每个B原子与3个氢原子成键,再与另一个B原子成键。但从B的价电子数来看,B2H6仅有12个价电子,而乙烷式构型需要14个价电子成键,况且B2H6与乙烷相比,化学、物理性质都有很大差别。因此有人提出硼烷应是桥式结构,即每个B原子与2个H原子形成B-H键,还与2个H原子形成桥键,桥键中的H原子只有一个价电子,如何可形成2个共价键,也不好处理。Lipscomb支持桥式结构,他认为2个B与一个H形成的桥键是双电子三中心键,而不是2个B-H键。后来电子衍射测定出气态中与晶体中的B2H6确实是桥式的结构。B与两端的H原子的B-H键键长是119.2pm,B与H
形成的桥键键长达132.9pm
|
|
|
|
(1)现在普遍被接受的观点是:B2H6中的B以sp3杂化参与成键,每个B原子与2个H原子形成普通的B-H键,剩余的2个杂化轨道与1个电子、与另一个同样的B原子、2个H桥原子形成2个三中心键,即缺电子原子的特殊共价键形式--三中心双电子键。除了B2H6以外,还有许多硼烷,这些化合物中有3种类型的化学键
|
|
(a) 正常的共价单键,如B-H,B-B
|
|
(b) 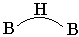 、 、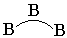 、桥键, 、桥键,
|
|
(c) 两个以上的B原子形成的多中心键
|
|
(2)巢状硼烷B5H9,5个B原子形成四方锥骨架,每个B原子形成一个B-H键,四方锥底的4个B还两两与氢形成3中心双电子键 ,锥底每个B原子还有一个价电子,锥顶B原子还有2个价电子,形成一个5中心的6电子键--即四方锥骨架。 ,锥底每个B原子还有一个价电子,锥顶B原子还有2个价电子,形成一个5中心的6电子键--即四方锥骨架。
|
| 
三中心两电子氢桥键
|
三中心两电子硼桥键 |
三中心两电子硼键 |
五中心六电子硼键 |
图6-1 几种缺电子多中心键形式
|
|