|
五、Pauli不相容原理
在同一原子轨道或分子轨道上,至多只能容纳两个电子,这两个电子的自旋状态必须相反。或者说两个自旋相同的电子不能占据相同的轨道。
十九世纪末二十世纪初,Zeeman,Stern等分别在光谱实验中发现: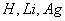 等只含1个价电子的原子光谱经过一个不均匀磁场后,谱线分为
2条。光谱的精细结构说明:电子除了空间轨道运动外还有其它运动。1925年乌仑贝克(Whlenbeck)和哥希密特(Goldschmidt)提出电子自旋的假设,认为电子具有自旋运动,具有固定的角动量和相应的磁距。描述电子运动的状态波函数除了包括空间坐标外,还包括自旋坐标(s)。一个含有N个电子体系的完全波函数(定态)是: 等只含1个价电子的原子光谱经过一个不均匀磁场后,谱线分为
2条。光谱的精细结构说明:电子除了空间轨道运动外还有其它运动。1925年乌仑贝克(Whlenbeck)和哥希密特(Goldschmidt)提出电子自旋的假设,认为电子具有自旋运动,具有固定的角动量和相应的磁距。描述电子运动的状态波函数除了包括空间坐标外,还包括自旋坐标(s)。一个含有N个电子体系的完全波函数(定态)是:
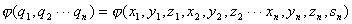
在经典力学中,一些全同粒子可能有相同的质量,相同的电量等,但宏观粒子在运动中都有自己的运动轨道,任何时刻可用粒子在空间的坐标和动量来标记它们。虽然性质相同,但还是可以区别的。但在量子力学里,一些微观粒子,如一组电子,一组光子等,它们具有相同的质量,电量,自旋等,它们具有波粒二象性,服从“测不准原理”,在这样的全同粒子体系中,粒子是彼此不可区分的,当它们之间任意两个交换时,不会造成任何可观察的结果。例如一个由2个电子组成的体系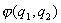 ,用 ,用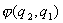 表示两个电子交换后的状态,根据不可区分性 表示两个电子交换后的状态,根据不可区分性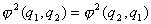 ,这样 ,这样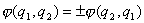 ,对取正号的函数称之为对称函数,取负号的函数为反对称函数。 ,对取正号的函数称之为对称函数,取负号的函数为反对称函数。
|